
2. Йодометрический метод для медноцинковых сплавов, не содержащих олова
Вариант А
Сущность метода. Метод основан на реакции окисления йодида калия ионом двухвалентной меди по уравнению:
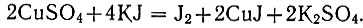
Выделившийся при этом свободный йод титруют раствором серноватистокислого натрия, который восстанавливает его до йодидиона по реакции:
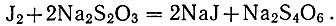
Медь от сопутствующих элементов отделяют тиосульфатом натрия. При действии тиосульфатом двухвалентная медь вначале восстанавливается до одновалентной с образованием комплексной соли:
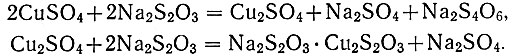
Неустойчивая комплексная соль при кипячении разлагается , с выделением полусернистой меди:
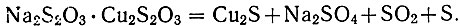
Реактивы. Натрий серноватистокислый, 0,1-н. титрованный раствор. Титр серноватистокислого натрия устанавливают по двухромовокислому калию.
0,2 г двухромовокислого калия, высушенного при температуре 180°С, помещают в коническую колбу емкостью 300 см3, прибавляют 100 см3 воды, 10 см3 соляной кислоты (1:1) и растворяют на холоду. Прибавляют 5 г йодистого калия, перемешивают, выдерживают в темном месте 2-3 мин и выделившийся йод титруют 0,1-н. раствором серноватистокислого натрия. Перед концом титрования прибавляют 2-3 см3 свежеприготовленного раствора крахмала (5 г/л) и титруют до исчезновения синей окраски крахмала. Титр раствора серноватистокислого натрия вычисляют по формуле:
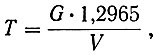
где T - титр раствора серноватистокислого натрия, выраженный в г меди;
V - количество раствора серноватистокислого натрия, израсходованное на титрование двухромовокислого калия, см3;
1,2965 - множитель для пересчета двухромовокислого калия на медь;
G - навеска двухромовокислого калия, г.
Выполнение определения. Навеску 0,2 г образца помещают в стакан емкостью 500 см3, прибавляют 5 см3 азотной кислоты (плотность 1400 кг/м3), 5 см3 серной кислоты (1:1) и растворяют при нагревании. Обмывают стенки стакана водой и выпаривают до паров серной кислоты. Последнюю операцию повторяют дважды. Охлаждают, соли растворяют в воде и разбавляют водой до объема 200 см3, нагревают раствор до кипения, прибавляют 60-80 см3 раствора серноватистокислого натрия (500 г/л) и кипятят до просветления раствора. Фильтруют на быстрофильтрующий фильтр и промывают 8-10 раз горячей водой. Фильтр с осадком помещают в фарфоровый тигель, подсушивают и прокаливают при температуре 500°С, остаток в тигле растворяют в 5 см3 азотной кислоты (плотность 1400 кг/м3), прибавляют 5 см3 серной кислоты (1:1) и дважды выпаривают до паров серной кислоты. Раствор переносят из тигля в коническую колбу емкостью 500 см3, прибавляют воды до объема 200 см3, 5 г йодистого калия, выдерживают в темном месте в течение 3-5 мин и титруют выделившийся йод 0,1-н. раствором серноватистокислого натрия до светложелтой окраски. Прибавляют 3-5 см3 свежеприготовленного раствора крахмала (5 г/л) и медленно, при перемешивании, титруют до исчезновения синей окраски крахмала.
Конец титрования наблюдают по окраске, которая бледнеет после прибавления каждой капли тиосульфата, до тех пор, пока от одной капли раствор не окрасится в молочно-розовый цвет.
Процентное содержание меди вычисляют по формуле:
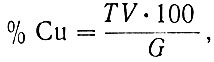
где Т - титр раствора серноватистокислого натрия, выраженный в г меди;
V - количество раствора серноватистокислого натрия, израсходованное на титрование, см3;
G - навеска образца, г.
Вариант Б
Сущность метода. Метод основан на йодометрическом определении меди в присутствии сопутствующих компонентов - железа, сурьмы, мышьяка и других элементов.
Влияние железа устраняют действием фторидами натрия или аммония с образованием комплексного соединения состава: K3[FeF6] или (NH4)3[FeF6]. Ион [FeF6]3- не реагирует с йодистым калием с выделением йода. Мышьяк и сурьма должны находиться в окисленной пятивалентной форме.
Реактивы. Натрий серноватистокислый, 0,1-н. титрованный раствор. Титр серноватистокислого натрия устанавливают по двухромовокислому калию.
Выполнение определения. Навеску 0,2 г образца помещают в коническую колбу емкостью 500 см3, прибавляют 5 см3 азотной кислоты (плотность 1400 кг/м3) и нагревают до полного растворения образца, обмывают стенки колбы водой и кипятят до удаления окислов азота. Раствор охлаждают и нейтрализуют аммиаком (плотность 900 кг/м3) до образования основных солей меди, которые затем растворяют полностью, прибавляя по каплям азотную кислоту (1:5), не вводя ее в избыток. Прибавляют 2-3 г фтористого натрия для связывания присутствующего иона Fe3+ в комплекс, 5 г йодистого калия и заканчивают анализ, как описано в варианте А.
|
ПОИСК:
|
© METALLURGU.RU, 2010-2020
При использовании материалов сайта активная ссылка обязательна:
http://metallurgu.ru/ 'Библиотека по металлургии'
При использовании материалов сайта активная ссылка обязательна:
http://metallurgu.ru/ 'Библиотека по металлургии'