
Металлы сегодняшнего дня
Для признания металла необходим его тесный союз с техникой. Но не у каждого металла судьба складывается так счастливо, как у алюминия: дав крылья авиации, он и сам поднялся на недоступные раньше высоты. Наивно было бы думать, что, как только ученый приносит в мир техники новый металл, конструкторы сразу находят применение его необыкновенным свойствам.
Тугоплавкий (температура плавления больше 3000°С), кислотоупорный и высокопрочный металл тантал был открыт в 1802 году (по признанию автора Экеберга, "с танталовыми муками"?!), а получен в чистом виде только спустя столетие. Более полувека "пылился" тантал на полочке "чистой науки", пока "сверхтехника" нашего времени не потребовала от материалов "сверхвозможностей". К примеру, сопла ракет и межпланетных кораблей выбрасывают раскаленные газы, температура которых достигает 3300°С! Для охлаждения их в полете применяются так называемые криогенные жидкости - вещества, основу которых составляют расплавленные щелочи; перепад температуры в процессе охлаждения составляет 1425°С. И все же нашлось вещество, способное стабильно работать и в этом аду, - карбид тантала.
В походе (а тем более в полете!) весит и иголка! А танталовые конденсаторы в радиоаппаратуре ракет и спутников имеют микроминиатюрные размеры. Цветной телевизор - достойный потребитель этого ультрасовременного металла на Земле. Тантал обнаруживает и еще одно необычное свойство: он сживается с тканями организма!
Танталовыми нитями можно сшивать сухожилия, нервы, сосуды, на танталовую сетку наращивается живая мускульная ткань, из тантала моделируют кости черепа и позвоночника.
Во всех природных соединениях тантала вместе с ним присутствует и его "двойник" - ниобий. Виднейшие химики XIX века (Берцедиус, Экеберг и другие) около 40 лет колебались - имеют они дело с одним или с двумя элементами. Поэтому элемент периодической системы № 41 больше века имел два названия: колумбий, данное ему первооткрывателем Чарльзом Гатчеттом (минерал, содержащий колумбит, был привезен из Америки), и ниобий, полученное при втором рождении 43 года спустя от Генриха Розе, сумевшего убедить научный мир в существовании двух сходных, но самостоятельных элементов.
По идее Розе, название "ниобий" подчеркивало родственные отношения элемента с танталом, равно как и его горестную судьбу (в античной мифологии страдалица Ниобея, потерявшая в течение одного дня шестерых сыновей и шестерых дочерей, приходилась родной дочерью титану Танталу).
Лишь в 1950 году Международный союз чистой и прикладной химии утвердил за элементом название ниобий, оставив название колумбит за минералом, в котором он впервые был установлен.
Но трудная судьба ниобия не изменилась с его вторичным и окончательным рождением. Оказалось, что при всей близости свойств ниобий всегда несколько уступает своему более удачливому двойнику: температура его плавления высока (2460°С), но ниже, чем у тантала, устойчивость против агрессивных химических реагентов и биологических сред велика, но меньше, чем у тантала.
Нашлись, однако, и у ниобия преимущества перед танталом: в природе его почти в 10 раз больше, чем тантала, значит, он гораздо дешевле, а кроме того, он в два раза легче тантала. Теперь металлургия, которой тантал несколько "не по карману", применяет ниобий для легирующих добавок. Добавки ниобия придают стали не только антикоррозионные свойства, термостойкость, жаропрочность, но и улучшают ее сварочные свойства, что особенно ценно при изготовлении труб большого диаметра (для газопроводов). Медь с примесью ниобия становится тверже при высоких температурах, молибден, титан и цирконий также приобретают жаростойкость и жаропрочность. Сплавы олова и других металлов с ниобием является сверхпроводником.
Естественно, такой набор "личных" качеств вызывает интерес к этому металлу не только у металлургии, но и у таких современных отраслей, как авиация, ракетная и космическая техника, химическое машиностроение. Уникальное свойство ниобия - отсутствие заметного взаимодействия с ураном при температуре до 1100°С - позволяет использовать его в атомном машиностроении и в качестве защиты от радиации, а устойчивость к биосредам - в восстановительной хирургии.
Элементы-родственники тантал и ниобий неразлучны в природе - нет минералов тантала, не содержащих ниобий, как нет минералов ниобия, не имеющих хотя бы примеси тантала. Почти 90% всех известных минералов тантала и ниобия составляют тантало-ниобаты - сложные окислы тантала и ниобия. Черные, темно-коричневые, реже красновато-коричневые и бурые тантало-ниобаты характеризуются еще и специфическим смолистым блеском поверхности излома. Они отличаются также большей плотностью и накапливаются в россыпях. Чаще всего можно наблюдать их в виде мелких зерен, рассеянных в породе или группирующихся в виде нечетких слоев и линз.
Основными рудными минералами тантало-ниобатов являются лишь немногие*: колумбит (танталит) (рис. 43), пирохлор (микролит или гатчеттолит), воджинит и лопарит. Кристаллики тантало-ниобатов обычно очень мелки (1 - 2 миллиметра, а часто и десятые доли миллиметра). Пирохлор и его тантал содержащие родственники образуют октаэдры или реже кубы; для лопарита характерны взаимопрорастающие кубические кристаллы - "лопаритовые двойники"; колумбит и танталит образуют мелкие уплощенные призматические кристаллы с острой головкой, но в пегматитовых жилах встречаются сростки танталита до 5 и даже до 10 - 20 см.
* (В скобках даны танталовые разности.)

Рис. 43. Кристалл танталита
Пристальное внимание к ниобию и танталу минералогов и геологов во всем мире, отмечающееся в последнее десятилетие, привело к уточнению доли этих элементов в земной коре. Кларк ниобия (процентное содержание в земной коре) увеличился с 1939 года почти в десять раз!
Если ниобий долго жил под двумя названиями, то молибден навеки остался под чужим именем! Металл молибден был назван по минералу молибдениту - это логично. Но сам-то молибденит назван так явно по недоразумению - слово "молибдос" означает по- гречески свинец! В древности так называли не только свинец, но и свинчак (мелкозернистую свинцовую руду, разновидность галенита), а заодно и сходные серые зернистые мажущиеся камни - графит и молибденит.
Надо сказать, что в кристаллах все три минерала резко отличаются: галенит образует блестящие темно-серые кубики; молибденит кристаллизуется в виде несовершенных шестигранных табличек, гибких и мягких под пальцами, их легко можно расщепить ногтем на тонкие листочки и на пальцах при этом остается голубовато-серый, жирный на ощупь, порошок; графит же очень редко образует кристаллы. Но в мелкозернистом агрегате эти минералы очень похожи, и их путали не только античные и средневековые натуралисты и рудознатцы - до сих пор это "любимые" ошибки студентов.
Чтобы отличать эти минералы, нужен всего клочок бумаги. Галенит ее рвет (его твердость 2), а черта молибденита и графита отчетливо различаются по цвету. Свойство молибденита и графита хорошо чертить бумагу определило их специальность - в старину из них изготовляли карандаши. Молибденовых (так называемых свинцовых) голубовато-серых карандашей давно не делают. Пластичность молибденитовых чешуек используют при производстве высокотемпературных смазок (например, в деталях коробки передач в автомобилях).
Однако основная сфера деятельности молибдена - легирующие добавки к сталям. Близость кристаллической решетки железа и молибдена позволяет им образовывать твердые растворы, причем установлено, что даже незначительная добавка молибдена способствует медленному росту зерен стали в период кристаллизации металла, обеспечивая ему равномерную мелкозернистую структуру. Эта особенность молибденовой лигатуры дает великолепный эффект - с возрастанием твердости возрастает и вязкость металла. Недаром молибден долго называли "военным" металлом - броня танков и кораблей, стволы орудий, бронебойные снаряды - основные потребители молибденосодержащей стали. Только "военным" этот металл был задолго до появления танков и пушек - легендарные самурайские мечи, секрет которых хранился веками, содержали природную примесь молибдена.
В настоящее время основной потребитель молибденовых сталей - авиация. Жесткий каркас самолета состоит из металлических труб. При нынешних грандиозных размерах лайнеров требуются трубы значительного диаметра, но с малой толщиной стенок. Подобные трубы удалось сделать только из хромомолибденовой стали.
Серебристо-белый цирконий по праву может быть назван металлом атомного века. Одно из характерных свойств циркония - малое сечение поперечного захвата тепловых нейтронов позволяет ему претендовать на роль конструкционного металла ядерных реакторов.
Жаропрочность (температура плавления 1860°С) в соединении с коррозионной устойчивостью подтверждают справедливость претензий циркония. Если бы не одно "но". В природных соединениях цирконий всегда сопровождает гафний, во многом похожий на него, кроме главного - отношения к нейтронам (поперечное сечение захвата нейтронов у гафния очень высокое). И достаточно цирконию иметь полуторапроцентную примесь гафния, как его конструктивные возможности ухудшатся в 20 раз!
Немало пришлось потрудиться химикам и металлургам, прежде чем в атомных реакторах появились циркониевые оболочки стержней и другие конструкционные детали. Коррозионная устойчивость позволяет использовать цирконий в химическом машиностроении или, например, для такой ответственной и деликатной детали, как наконечник фильера, тянущего нить ацетатного шелка - кислая среда в этом процессе сменяется щелочной; лишь "весьма благородные" металлы способны вынести такие перемены.
Еще одна важная область применения циркония - современная металлургия, требующая стойкости и прочности от стали не только на воздухе, но и в коррозионных средах, не только при высоких, но и при низких температурах. В этих случаях небольшая доза "витамина Zr" оказывает магическое действие От добавки циркония не отказываются и цветные металлы - магниевые сплавы с цинком и цирконием отличаются очень высокими механическими свойствами при малом удельном весе и используются самолетостроителями.
Открыт цирконий в 1789 году в драгоценном цейлонском цирконе. Первооткрыватель этого элемента Клайпрот. Великолепные прозрачные и ярко сверкающие цирконы славились еще в древности. Весьма ценился этот камень и в Азии - библейские первосвященники среди двенадцати священных камней носили золотисто-красный циркон гиацинт. В средние века европейским ювелирам был известен драгоценный камень "несовершенный алмаз" - желтоватый прозрачный самоцвет действительно "играл" почти, как алмаз, лишь много позже выяснилось, что "несовершенные" или "матарские" (Матара район Шри Ланка) "алмазы" являются цирконами. Однако ювелирные цирконы - очень большая редкость.
Впрочем прозрачные и совершенные кристаллы часты даже в обычных гранитах, но, к сожалению, видны они только под микроскопом: эти "драгоценности" имеют размер десятые, а то и сотые доли миллиметра.
Мутноватые, прозрачные лишь в мелких осколках цирконы встречаются очень часто. Обычно они имеют изящный облик четырехгранной призмочки, завершенной с обоих концов пирамидами. Среди окрасок циркона преобладают красновато-коричневые или розовато-коричневые тона, иногда отмечаются сиренево-розовые, серо-голубые; в Японии описываются даже темно-зеленые и оливково-зеленые цирконы.
Минерал циркон подобно металлу цирконию отличается хорошими механическими и "антикоррозионными" свойствами и поэтому накапливается в россыпях. Россыпи - основной, почти единственный источник и второго, значительного более редкого минерала - бадделеита (двуокиси циркония). Но стоит поискать его - ведь это почти готовый для промышленного использования продукт. Многие отрасли промышленности могут употреблять двуокись циркония без переработки. Бадделеит в виде очень блестящих темно-бурых мелких и тонких призмочек извлекается и как ценная попутная примесь при разработке некоторых железорудных месторождений. Есть и другие еще более редкие минералы циркония. Может быть, в одной из уникальных минералогических кладовых - щелочных массивах Хибин - вам посчастливится найти янтарно-желтые лучистые агрегаты ловенита или мелкие золотистые призмочки велерита и уже наверняка - клюквенно-красные вкрапления эвдиалита - "лопарской крови".
Если танталу пришлось ждать своей судьбы полтораста лет, то бериллий терпел почти 5000 лет! Впрочем, как и в случае циркония, это касается именно металла, ибо соединения бериллия слава никогда не обходила. Пожалуй, нет такого второго элемента в периодической системе, который бы подарил людям столько самоцветов. Заглянем в золотую кладовую Эрмитажа: в залах скифского и причерноморского золота привычный глаз минералога сразу "выхватывает" естественные, граненные природой призмочки мелких изумрудов, нанизанных на витую золотую цепочку или подвешенных к золотой серьге. Знамениты по красоте изумруды Урала. С ними могут спорить лишь густо-зеленые камни Южной Америки - любимый "зеленый лед" инков. Испанцы вместе с золотом ввезли в Европу и изумруды Колумбии. И, наверное, никто не выразил идею покорения Нового Света так изящно и убедительно, как испанский ювелир XVIII века, вырезавший бегущую под распущенными изумрудными парусами каравеллу из цельного колумбийского изумруда весом более 120 карат. А как красивы нежно-розовый воробьевит, гелиодор, словно налитый медом и солнцем, чуть голубой и прозрачный, похожий на море в граненом стакане, аквамарин, знаменитый александрит - зеленый при солнце и лилово-малиновый при свете лампы, загадочный эвклаз - в его кристаллах голубизна словно тает на глазах, водянопрозрачные фенакиты, "игрой" не уступающие бриллиантам.
И все же сегодня нас больше поражает уникальность свойств чистого бериллия. Вдвое более легкий, чем алюминий, но теплостойкий и прочный, как лучшие сорта сталей, бериллий нашел широкое применение в авиации и космической технике. Именно из бериллия были выполнены носовая часть корпуса и днище космического корабля "Френдшип-70". Свыше 1000 деталей современного самолета сделаны из бериллиевой бронзы, не знающей усталости (до 20 миллиардов циклов нагрузки выдерживают "вечные" пружины из бериллиевой бронзы!).
Атомные реакторы, одно из грозных чудес нашего века, - еще один из основных потребителей бериллия. Создание их стало возможным лишь после того, как человек научился управлять потоками частиц, извергающихся при сгорании ядерного топлива! И именно элемент бериллий оказался способным замедлить скорость тепловых нейтронов, отразить их и возвратить в активную зону реактора. Бериллий - один из необходимых элементов в атомной технике. Полностью оправдал сегодня бериллий надежды, возложенные на него замечательным минералогом и геохимиком, энтузиастом освоения минеральных богатств нашей Родины А. Е. Ферсманом. "Бериллий - один из самых замечательных элементов огромного теоретического и практического значения... Мы уже предвидим, что в помощь современным металлам авиации - алюминию и магнию - придет и бериллий."
А как выглядят руды бериллия? Они содержат те же минералы - берилл, фенакит, эвклаз, но не в виде драгоценных камней. Долгое время разрабатывались лишь пегматитовые жилы с крупными кристаллами берилла (рис. 44), нередко до тонны, а в "Занимательной геохимии" А. Е. Ферсмана приводится фотография восемнадцатитонного берилла. Но аппетиты современной техники нельзя удовлетворить только за счет этих гигантских уникумов. Как показывает сегодняшний опыт эксплуатации месторождений, вполне выгодны (как говорят рентабельны) и крупные по запасам и габаритам рудные тела с мелкой вкрапленностью. Они возникают в процессе пропитки гранитных массивов рудоносными растворами.

Рис. 44. Руда с бериллом
И те же минералы здесь выглядят иначе. Кристаллизация из более холодных и более щелочных растворов изменила габитус кристаллов: излюбленные формы выделения фенакита здесь - шарообразные лучистые солнышки и розетки в ассоциации с лиловым флюоритом и розовым полевым шпатом (рис. 45), а берилла - тонкая светлая вкрапленность в руде. Еще труднее для диагностики руды, содержащие минералы прежде необычайно редкие - бертрандит, эвклаз, гентгельвин. Тут на помощь приходит "современное" поведение бериллиевых минералов: при поисках бериллиевых руд специальный прибор направляет на породу искусственное радиоактивное облучение и минералы бериллия, сразу дают о себе знать, излучая пучок нейтронов.

Рис. 45. Розетка фенакита в берилловой руде
Среди металлов сегодняшнего дня особое место занимает весьма своеобразный металл - литий. "Незаурядные" качества выдвигают его на первые призовые места среди металлов: литий первый по легкости - он в пять раз легче алюминия и в пятнадцать раз легче железа; первый по удельной теплоемкости, первый в ряду напряжения металлов, хотя на вид довольно обычный - серебристо-белый с ярким блеском, правда, очень мягкий (режется ножом!). Увидеть подлинный облик лития можно только в вакууме: на воздухе литий активно соединяется с азотом и кислородом и покрывается белой пленкой.
Естественно, уникальные свойства лития и его положение в периодической системе Менделеева влияют и на облик его природных соединений. Тут литий держит еще одно первенство, как самый литофильный элемент. Когда знаменитому шведскому химику Иенсу Якобу Берцелиусу молодой Арфведсон показал новый щелочной элемент, только что полученный из белого, похожего на полевой шпат камня, Берцелиус предложил назвать новую щелочь литионом. Со временем это имя трансформировалось в более короткое и современное - литий. Берцелиус очень точно угадал каменную душу элемента: большинство минералов лития - аналоги самых распространенных породообразующих минералов; среди них пироксен и амфибол, слюды и хлориты; структура этих минералов аналогична структуре их породообразующих аналогов, но только роль железа в них играет литий. Основной рудный минерал лития - пироксен сподумен (рис. 46). Сростки светло-серого, розоватого, а иногда зеленоватого или серо-желтого пироксена напоминают свалы досок - кристаллы в них плоские, часто сужаются к одному концу и обычно неровно, как щепки, обломаны в торце. Да и по размеру они часто не уступают доскам, а бывают; и больше. Со сподуменом в пегматитах часто соседствует тот самый изученный Арфведсоном петалит, напоминающий полевой шпат не только внешним видом, но и структурой, и сиреневая слюда лития лепидолит, и тяжелый белый или светло-серый фосфат лития - амблигонит, образующий в пегматите крупные гнезда с темно-серой оторочкой.
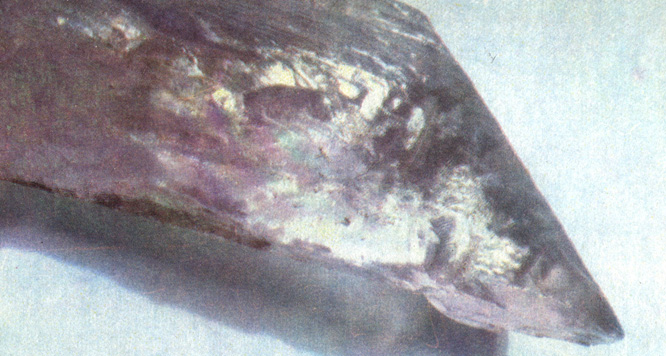
Рис. 46. Сподумен - кунцит
Мы знаем двадцать пять минералов лития, но промышленность использует пока только пять из них: прежде всего сподумен и лепидолит, а иногда петалит, амблигонит и тонкочешуйчатую темно- серую литиевую слюду - циннвальдит. Литий добывается также из природных рассолов - рапы соляных озер (попутно с солями натрия и магния). Характерно, что активный, энергичный литий не довольствуется своими двадцатью пятью минералами и при первой возможности забирается в кристаллические решетки таких породообразующих минералов, как полевые шпаты, пироксены и прежде всего слюды, вытесняя калий и натрий.
Уникальность свойств лития открывает возможность его применения в весьма специфических условиях. Известно, что при соединении ядер тяжелых изотопов водорода - дейтерия и трития - высвобождается колоссальная энергия. Эта термоядерная реакция лежит в основе водородной бомбы. Реакция проходит при температуре 50 миллионов градусов и в жидкой среде. Вещество, жидкое при такой температуре, - это дейтерид лития-6. Кроме того изотоп лития - литий-6 является единственным промышленным источником второго компонента реакции - самого дефицитного изотопа водорода - трития (бомбардировка лития-6 нейтронами приводит к возникновению трития и инертного газа гелия). Так в реакции термоядерного синтеза литий-6 играет "первую скрипку".
Много лет ученые во всем мире работают над тем, чтобы сделать эту реакцию управляемой. Решение данной проблемы позволило бы покончить с энергетическим кризисом. Пока же работу разного рода выполняет второй их значительно более распространенный изотоп лития - литий-7. Литий может служить прекрасным теплоносителем в мирных ядерных реакторах, большая разница между температурой плавления и кипения позволяет литию оставаться жидкостью в очень широком диапазоне температур.
И еще одна весьма современная способность: необычайно высокая теплотворная способность открывает перспективы использования лития как ракетного топлива на сверхдальних космических трассах.
А нет ли у лития более земной, повседневной работы? Есть. Высокая реакционная способность, сродство к водороду, азоту, кислороду позволяют литию проявить прекрасные способности дегазатора и раскислителя черных и цветных металлов. Сплав свинца с литием - банметалл, изобретенный взамен более дефицитного олова, служит хорошим антифрикционным материалом; алюминию литий придает повышенные антикоррозионные и механические свойства, а сверхлегкий, плавающий на воде, сплав лития с магнием - мечта авиаконструктора.
Интересные области применения находят неметаллические соединения лития. Современная химия разработала колоссальный спектр различных полимеров, подчас не уступающих, а часто превосходящих по свойствам такие традиционные материалы, как сталь, латунь, стекло. Но разрешить проблему соединения этих материалов с металлами и между собой - задача сложная. "Ядерным клеем" здесь служат соединения лития.
Гидрид лития - белое кристаллическое вещество - спас жизнь многим морякам и летчикам, потерпевшим аварию в море. Количество водорода, вырабатываемого этим соединением, столь велико, что одна-две таблетки при соединении с водой мгновенно наполняют газом плавучие средства - спасательные жилеты, плотики, сигнальные шары.
Органические соединения лития типа стеарита составляют основу смазочных материалов, уверенно работающих на морозе при температуре минус 60°С и на жаре при плюс 160°С! Идеальная смазка вездеходов, бороздящих Арктику, Африку и Антарктику! Не обходится без лития и современная астрономия - линзы из монокристалла фтористого лития прозрачны не только для лучей видимого спектра, но и для ультрафиолетовых лучей. А нас литий радует каждый праздник, когда вечернее небо расцветает огнями салюта: яркие сине-зеленые звездочки - огни сгорающих солей лития.
Золотисто-солнечный полужидкий металл цезий, живущий обычно в запаянных стеклянных капсулах, тоже мог бы лидировать в группе редких металлов, но совсем в других областях. Это первый элемент, открытый путем спектрального анализа. Собственно и свое название он получил по небесно-голубому цвету характерных для него спектральных линий ("цезиум" - небесно-голубой).
Цезий - второй по легкоплавкости после ртути (его температура плавления 28,5°С). Но главную роль в его судьбе играет слишком большой атомный радиус, не позволяющий ему занять место в кристаллических решетках минералов, поэтому цезий - рекордсмен по малочисленности природных соединений. Если литий образует 25 минералов, цирконий - около 30, бериллий - 43, а ниобий и тантал - около 90, то цезий концентрируется почти исключительно в одном алюмосиликате - поллуците, рыхлый каркас которого выдерживает его "громоздкие" ионы. Этот полупрозрачный или молочно-белый минерал чрезвычайно похож на кварц, на белый полевой шпат, а еще больше - на бесцветный берилл, и отличить его можно разве по обилию трещинок, по специфическим тонким серо-сиреневым прожилкам да по характерному искрящемуся блеску. Вместе со сподуменом, петалитом и лепидолитом поллуцит встречается в литиевых пегматитах, образуя угловатые глыбы - блоки между другими минералами. Плохо образованные кубические кристаллы были встречены только в пустотках пегматитов на острове Эльба, где они росли вместе с призматическими, тоже полупрозрачными и бесцветными кристаллами касторита.
Главное свойство элемента цезия, создающее ему имя в современной технике, - необычайно чуткая реакция на свет, в том числе на инфракрасные и ультрафиолетовые лучи. Потребности техники в цезии так стремительно растут из года в год, что геологи опасаются - сможет ли один поллуцит удовлетворить их.
Конечно, мы не можем рассмотреть все металлы и их минералы. Но уже беглый экскурс в мир "камней, рождающих металлы" - от первого кремня до руд тантала, бериллия, цезия, - поражает воображение богатством земных недр.
Ну, а как же наш первый камень прапредок всех руд? Неужели его место в музее в залах палеолита и неолита? Нет! Основа кремня - чистый кремний ("чистый" - это значит, что на его 999999 атомов может быть только один "чужой" атом!). Он прекрасный полупроводник, незаменимый в электронике. А "нечистый" кремний? Это - оконное стекло в вашем доме, бетон новостроек и, конечно, прекрасные самоцветы - лиловый аметист, дымчатый раухтопаз, горный хрусталь, прихотливо мерцающий опал и все халцедоны, агаты, яшмы и кремни самых невероятных цветов и оттенков.
|
ПОИСК:
|
© METALLURGU.RU, 2010-2020
При использовании материалов сайта активная ссылка обязательна:
http://metallurgu.ru/ 'Библиотека по металлургии'
При использовании материалов сайта активная ссылка обязательна:
http://metallurgu.ru/ 'Библиотека по металлургии'