
Методы определения хрома в сплавах на медной основе
1. Объемный персульфатносеребряный метод с фенилантраниловой кислотой в качестве индикатора
Без отделения меди
Сущность метода. Метод основан на окислении хрома в хромат-ион в сернокислом растворе действием надсернокислого аммония в присутствии катализатора - азотнокислого серебра.
Уравнение реакции:
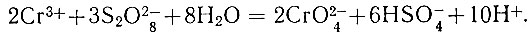
Хромат-ион титруют раствором двойной сернокислой соли закиси железа-аммония в присутствии индикатора-фенилантраниловой кислоты.
Уравнение реакции:
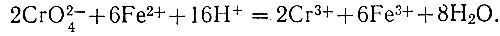
Титрование производят на фоне основного компонента меди.
Реактивы. 1. Калий двухромовокислый, перекристаллизованный и просушенный при температуре 180-200°С.
2. Титрованный раствор двойной сернокислой соли закиси железа-аммония (0,034-н.): 12 г соли растворяют в 300 см3 воды, содержащей 20 см3 серной кислоты (плотность 1840 кг/м3), разбавляют до литра водой и перемешивают.
Установка титра раствора двойной сернокислой соли закиси железа-аммония:
а) по двухромовокислому калию. Для установки титра раствора двойной сернокислой соли закиси железа аммония берут три навески по 0,05 г двухромовокислого калия, перекристаллизованного и просушенного при температуре 180-200°С в течение 2 ч; растворяют в 150-200 см3 воды, приливают 60 см3 разбавленной серной кислоты (1:4), б капель фенилантраниловой кислоты и титруют раствором двойной сернокислой соли закиси железа-аммония до перехода сине-фиолетовой окраски раствора в зеленую. Титр раствора двойной сернокислой соли закиси железа-аммония, выраженный в граммах хрома, вычисляют по формуле:
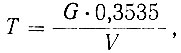
где Т - титр раствора двойной сернокислой соли закиси железа-аммония, выраженный в г хрома;
G - навеска двухромовокислого калия, г;
V - количество см3 раствора двойной сернокислой соли закиси железа-аммония;
0,3535 - множитель для пересчета двухромовокислого калия на хром;
б) по стандартному образцу. Для установки титра раствора двойной сернокислой соли закиси железа-аммония берут стандартный образец, аналогичный по содержанию хрома, и проводят через все стадии анализа.
Титр раствора двойной сернокислой соли закиси железа-аммония вычисляют по формуле:
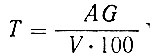
где Т - титр раствора двойной сернокислой соли закиси железа-аммония, г;
А - процентное содержание хрома в стандартном образце;
G - навеска стандартного образца, г;
V - количество см3 раствора сернокислой соли закиси железа-аммония, израсходованное на титрование хрома, содержащегося во взятой навеске стандартного образца.
Выполнение определения. Навеску 1 г образца помещают в коническую колбу емкостью 500 см3, растворяют в 25 см3 разбавленной азотной кислоты (1:1). По растворении навески прибавляют 10 см3 серной кислоты (плотность 1840 кг/м3) и выпаривают до выделения паров серной кислоты. По охлаждении соли растворяют в 120 см3 воды, прибавляют 5-10 см3 фосфорной кислоты (плотность 1700 кг/м3) и разбавляют водой до объема 250 см3. Раствор нагревают до кипения, прибавляют 10 см3 раствора азотнокислого серебра (2,5 г/л), 1-2 капли раствора сернокислого марганца (2 г/л), 20 см3 раствора надсернокислого аммония (300 г/л) и кипятят несколько минут. При этом трехвалентный хром окисляется до хромат-иона, а марганец - до манганат-иона, вследствие чего раствор окрашивается в малиновый цвет, что указывает на полноту окисления хрома. К кипящему раствору прибавляют 5 см3 хлористого натрия (50 г/л) и кипятят до исчезновения окраски марганцевой кислоты и до полной коагуляции хлористого серебра. Раствор охлаждают до комнатной температуры (15-20°С), прибавляют 60 см3 разбавленной серной кислоты (1:4), 6 капель фенил-антраниловой кислоты и медленно титруют раствором двойной сернокислой соли закиси железа-аммония до перехода грязновато-фиолетовой окраски в зеленую.
Процентное содержание хрома вычисляют по формуле:
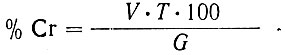
где V - количество см3 раствора двойной сернокислой соли закиси железа-аммония;
Т - титр раствора двойной сернокислой соли закиси железа-аммония, выраженный в г хрома;
G - навеска образца, г.
С предварительным отделением меди
Сущность метода. После отделения меди электролизом хром окисляют до хромат-иона действием надсернокислого аммония. Хромат-ион титруют раствором двойной сернокислой соли закиси железа-аммония в присутствии индикатора - фенилантраниловой кислоты.
Реактивы. Те же, что и для метода определения хрома без отделения основного компонента меди.
Выполнение определения. Навеску 1 г образца помещают в стакан емкостью 300 см3 и растворяют в 25 см3 разбавленной азотной кислоты (1:1). По окончании растворения прибавляют 20 см3 разбавленной серной кислоты (1:1) и выпаривают до выделения паров серной кислоты, до полного разрушения черных частиц карбидов хрома. По охлаждении, соли растворяют в 100 см3 воды, прибавляют аммиак (плотность 900 кг/м3) до начала впадения осадка основной соли меди, который растворяют в разбавленной азотной кислоте (1:1). Прибавляют 4 см3 разбавленной серной кислоты (1:1), 8 см3 разбавленной азотной кислоты (1:1), раствор нагревают до кипения, кипятят в течение 5-6 мин (до полного удаления окислов азота) и ставят на электролиз, который проводят при силе тока 1,5-2 а в течение 3-4 ч.
По окончании электролиза к электролиту прибавляют 10 см3 фосфорной кислоты (плотность 1700 кг/м3), раствор переводят в коническую колбу емкостью 500 см3, разбавляют водой до объема 250-300 см3 и дальнейший анализ проводят по методике определения хрома без отделения основного компонента.
|
ПОИСК:
|
© METALLURGU.RU, 2010-2020
При использовании материалов сайта активная ссылка обязательна:
http://metallurgu.ru/ 'Библиотека по металлургии'
При использовании материалов сайта активная ссылка обязательна:
http://metallurgu.ru/ 'Библиотека по металлургии'